Therapeutische koolhydraatbeperking bij diabetes type 1: historisch perspectief, richtlijnpositie en klinische implicaties
Vanwege positieve effecten op glucoseregulatie en metabole gezondheid staat therapeutische koolhydraatbeperking bij diabetes type 1 opnieuw in de belangstelling. Dit artikel bespreekt de historische achtergrond, de huidige richtlijnpositie en de klinische implicaties van therapeutische koolhydraatbeperking bij diabetes type 1. Het artikel richt zich op zorgprofessionals en op mensen met diabetes type 1 met inhoudelijke interesse in voedingsstrategieën. Toepassing in de praktijk vraagt om professionele begeleiding.

1. Inleiding
Wat zijn de mogelijkheden van therapeutische koolhydraatbeperking bij diabetes type 1 (DM1)? Het beperken van koolhydraten wordt steeds vaker besproken als mogelijke strategie voor volwassenen om schommelingen in glucosewaarden (glykemische variabiliteit) te beïnvloeden [1]. Richtlijnen erkennen koolhydraatbeperking als een passend voedingspatroon binnen de diabeteszorg, mits gebaseerd op volwaardige voeding, en formuleren geen specifieke ondergrens voor koolhydraatinname [2,6].
Historisch gezien maakte beperking van de koolhydraatinname deel uit van de medische behandeling van DM[1], zowel vóór als na de introductie van insuline. Met de ontwikkeling van intensieve insulinetherapie verschoof de nadruk naar het afstemmen van insulinedoseringen op variabele koolhydraatinname. Daarmee verloor koolhydraatreductie zijn positie als standaard dieetbehandeling, terwijl koolhydraattelling een centrale plaats kreeg binnen het zelfmanagement [2].
Van de voedingspatronen die bij DM[1] als passend worden beschouwd, is koolhydraatreductie het meest onderzocht in relatie tot de glucoserespons na de maaltijd en Time in Range. Daarbij worden in verschillende studies verbeteringen in glykemische uitkomsten beschreven, maar het beschikbare bewijs is beperkt in omvang en methodologisch heterogeen [3,4]. Richtlijnen benadrukken dat bij substantiële koolhydraatreductie zorgvuldige medicatie-aanpassing noodzakelijk is en dat bij sterke beperking aandacht moet worden besteed aan het risico op hypoglykemie en ketoacidose. Professionele begeleiding is daarbij het uitgangspunt [5].
In dit artikel wordt therapeutische koolhydraatbeperking (TKB) bij DM[1] besproken in historisch, richtlijn- en farmacologisch perspectief. De centrale vraag is niet of insuline vervangen kan worden, dat kan niet, maar onder welke klinische omstandigheden TKB onderdeel kan zijn van een integrale behandeling, en onder welke voorwaarden dit verantwoord kan worden toegepast.
2. Kernpunten
- Koolhydraatreductie heeft een lange geschiedenis als voedingstherapie bij DM1 en krijgt opnieuw klinische en wetenschappelijke aandacht.
- Richtlijnen erkennen meerdere voedingspatronen bij DM1, waaronder koolhydraatbeperkt en formuleren geen minimale koolhydraatinname.
- De toename van overgewicht en insulineresistentie binnen de DM1-populatie vormt een relevante klinische context voor hernieuwde aandacht.
- Onderzoek naar koolhydraatreductie bij DM1 suggereert minder glykemische variabiliteit, verlaagd HbA1c, meer TIR, gewichtsverlies en gereduceerde insulinebehoefte. Hoewel observationele data veelbelovend zijn, ontbreekt het vooralsnog aan grootschalig langdurig bewijs uit dubbelblinde studies (RCT’s) om de effecten definitief te bevestigen.
- Minder koolhydraten betekent een verschuiving naar meer eiwit en vet, wat de glucoserespons na de maaltijd en de benodigde insuline beïnvloedt.
- Sterke koolhydraatreductie vereist specialistische begeleiding, monitoring en zorgvuldige insuline afstemming.
- Insuline blijft altijd noodzakelijk bij DM1.
3. Historisch perspectief: medische voedingstherapie als oorsprong
Het beperken van de koolhydraatinname behoort tot de oudste behandelstrategieën bij DM[1]. De zogeheten starvation therapy, beschreven door Frederick M. Allen, was gericht op het beperken van hyperglykemie, het voorkomen van ketoacidose en het verlengen van overleving in een periode waarin geen farmacologische behandeling beschikbaar was [7]. In dezelfde periode beschreef Elliott P. Joslin dieetstructuren met vaste eettijden en een relatief stabiele koolhydraatinname, afgestemd op de beschikbare behandelmogelijkheden [8].
In 1921 beschreef dr. Russell M. Wilder (Mayo Clinic) een ketogeen dieet als therapeutische interventie bij zowel DM[1] als epilepsie [9]. Voor epilepsie is het ketogeen dieet tot op heden een erkende medische voedingstherapie; bij DM[1] verloor deze benadering geleidelijk terrein na de introductie en verdere verfijning van insulinebehandeling, waarbij farmacotherapie de dominante behandelmodaliteit werd. Desondanks bleef een gematigd koolhydraatbeperkt dieet tot ver in de twintigste eeuw gebruikelijk. Voeding en insuline waren in deze benadering nauw op elkaar afgestemd.
Met de introductie en wetenschappelijke onderbouwing van intensieve insulinetherapie verschoof de nadruk in de diabeteszorg vanaf de jaren tachtig naar farmacologische regulatie [10]. Insulinedoseringen werden afgestemd op variabele koolhydraatinname per maaltijd, in plaats van op vaste hoeveelheden koolhydraten en vaste maaltijdmomenten. In dezelfde periode ontwikkelden voedingsrichtlijnen zich richting hogere proporties koolhydraten binnen het voedingspatroon, terwijl koolhydraatreductie geleidelijk zijn positie als standaardtherapie verloor [1].
In de jaren zeventig werd een zeer koolhydraatbeperkte benadering beschreven en klinisch uitgewerkt door dr. Richard K. Bernstein (1934-2024), zelf arts en persoon met DM[1,11]. Zijn methode, gericht op minimalisering van de glucoserespons na de maaltijd door zeer lage koolhydraatinname en nauwkeurige insulineafstemming, werd uitgebreid beschreven in Dr. Bernstein’s Diabetes Solution en bleef invloedrijk binnen zelfmanagementpraktijken en online communities.
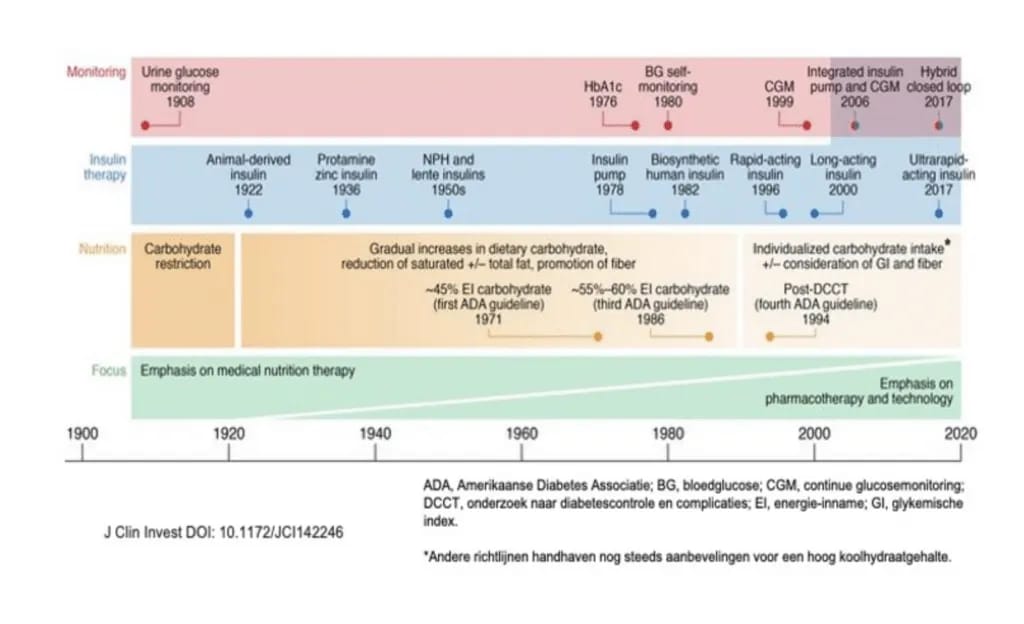
Het observationele onderzoek van Lennerz et al. (2018), uitgevoerd onder leden van een online community die een zeer koolhydraatarm voedingspatroon volgden, beschreef opvallend lage HbA1c-waarden en beperkte glykemische variabiliteit [12]. De onderzochte populatie was grotendeels geïnspireerd door de door Bernstein beschreven benadering. De studie was gebaseerd op zelfselectie en zelfrapportage en werd niet als onderbouwing opgenomen in richtlijnen of meta-analyses, maar illustreert de blijvende interesse in sterke koolhydraatreductie binnen de klinische en wetenschappelijke discussie. Een latere publicatie van Lennerz et al. (2021) plaatst koolhydraatbeperking in het bredere therapeutische kader van DM[1] en toont hoe de focus in de afgelopen eeuw verschoof van voeding naar farmacotherapie en technologie (zie figuur) [1]
4. Wat is therapeutische koolhydraatbeperking?
Therapeutische koolhydraatbeperking (TKB) is een leefstijlbehandeling die zich richt op het verbeteren van de metabole gezondheid door de inname van koolhydraten doelgericht te beperken. TKB wordt beschreven in de klinische richtlijnen van de Society of Metabolic Health Practitioners als een interventie voor metabole aandoeningen, waarbij de mate van koolhydraatbeperking afhankelijk is van de gezondheidstoestand en de individuele doelstellingen van de patiënt [13].
Binnen TKB worden twee niveaus onderscheiden:
- Matige koolhydraatbeperking: 50–130 gram koolhydraten per dag
- Sterke koolhydraatbeperking: minder dan 50 gram koolhydraten per dag
TKB richt zich op een hoge inname van natuurlijke, onbewerkte voedingsmiddelen, met een uitgebalanceerde verdeling van macro- en micronutriënten. Een lagere koolhydraatinname gaat gepaard met een relatieve toename van eiwit- en vetinname, waardoor het glucose verloop na de maaltijd verandert. Koolhydraten veroorzaken doorgaans een directe stijging van de bloedglucose, terwijl eiwitten via glucagonstimulatie en gluconeogenese een vertraagde stijging kunnen geven en vetten via vrije vetzuren en glycerol bijdragen aan een latere en soms langdurigere glucoserespons na de maaltijd.
Continue glucosemonitoring heeft deze verschillen in tijdsdynamiek zichtbaar gemaakt en onderstreept dat insulineafstemming bij DM[1] idealiter rekening houdt met alle drie de macronutriënten [14-17]. Deze macronutriëntverschuiving vormt de fysiologische basis voor aanpassing van de insulinetherapie bij TKB bij mensen met DM[1].
5. Waarom therapeutische koolhydraatbeperking bij diabetes type 1?
DM[1] werd lange tijd primair geassocieerd met een slank fenotype. De afgelopen decennia is echter een duidelijke toename van overgewicht en insulineresistentie zichtbaar binnen deze populatie. In meerdere regio’s lijkt de prevalentie van overgewicht onder jongeren met DM[1] vergelijkbaar met of hoger dan in de algemene bevolking, al bestaat hierover nog geen volledige consensus [18-21].
Intensieve insulinetherapie, noodzakelijk voor optimale glucoseregulatie, is in verschillende studies geassocieerd met gewichtstoename [22,23]. Daarnaast worden hogere BMI-waarden bij adolescenten in verband gebracht met een verhoogde incidentie van DM[1,24]. Deze ontwikkelingen spelen zich af binnen een obesogene omgeving, waarin hoge beschikbaarheid van energierijke, sterk bewerkte voeding en sociaal-economische factoren bijdragen aan gewichtstoename [20].
Overgewicht beïnvloedt de metabole regulatie bij DM[1]. Verminderde insulinegevoeligheid leidt tot hogere insulinebehoefte, wat kan bijdragen aan verdere gewichtstoename. Bovendien verhoogt de combinatie van DM[1] met kenmerken van het metabool syndroom – obesitas, hypertensie en dyslipidemie – het cardiovasculaire risico [20,23,25,26].
Deze combinatie wordt aangeduid als dubbele diabetes. In een Duitse cohortstudie onder 31.119 mensen met DM[1] had 25,5% kenmerken van het metabool syndroom. In deze groep was, onafhankelijk van de glucoseregulatie, zowel micro- als macrovasculaire comorbiditeit verhoogd [27]. De wisselwerking tussen gewichtstoename en toenemende insulinebehoefte kan zo een vicieuze cirkel vormen.
Grote cohortstudies zoals DCCT/EDIC laten zien dat intensieve behandeling complicaties reduceert, maar tevens gepaard kan gaan met verhoogde behandel belasting en gewichtstoename [22,23]. Naast gewichtstoename en insulineresistentie blijft ook de dagelijkse glucoseregulatie voor veel mensen met DM[1] een uitdaging. Ondanks intensieve insulinetherapie en moderne technologie, waaronder continue glucosemonitoring, behaalt een meerderheid van de mensen met DM[1] niet duurzaam de aanbevolen streefwaarden [28]. Daarnaast rapporteren mensen met DM[1] frequent hypo-angst en psychosociale belasting gerelateerd aan voortdurende zelfregulatie [29].
Deze combinatie van gewichtstoename, insulineresistentie, glykemische variabiliteit en hoge zelfmanagement belasting verklaart waarom naast farmacologische optimalisatie ook leefstijlinterventies worden verkend binnen een integraal behandelplan [20,30]. TKB kan in dat kader worden beschouwd als een gerichte voedingsstrategie, met mogelijke effecten op zowel glucoseregulatie als gewicht-gerelateerde uitkomsten.
6. Richtlijnen en onderzoek: wat is bekend?
Onderzoek naar koolhydraatreductie bij DM[1] laat zien dat zowel matige als sterke beperking gepaard kan gaan met meer Time in Range, minder glykemische variabiliteit en een lagere dagelijkse insulinebehoefte. De gerapporteerde effecten verschillen per populatie en mate van beperking.
6.1 Matige koolhydraatreductie (50–130 g/dag)
Binnen deze bandbreedte is het meeste onderzoek beschikbaar. De NDF Voedingsrichtlijn (2023) verwijst naar een meta-analyse waarin bij volwassenen met DM[1] bij koolhydraatbeperkte voeding gemiddeld circa één uur per dag meer Time in Range werd gevonden, met een lichte reductie van Time Below Range en verbetering van glykemische variabiliteit [4].
Systematische reviews en interventiestudies binnen deze categorie rapporteren over het algemeen bescheiden maar consistente verschuivingen in glykemische parameters. Er worden lichte dalingen in HbA1c beschreven, reducties in totale dagelijkse insulinedosering (in de orde van grootte van 8–20%) en verbeteringen in glykemische variabiliteit [31,32]. In sommige cohorten worden daarnaast geringe dalingen in triglyceriden en een beperkte gewichtsafname gezien [33].
De duur van de meeste interventies varieert van enkele weken tot enkele maanden. Langetermijneffecten op cardiovasculaire uitkomsten, complicaties en duurzaamheid van het voedingspatroon zijn niet systematisch onderzocht.
6.2 Sterke koolhydraatreductie (<50 g/dag)
Voor zeer koolhydraatarme of ketogene voeding bij DM[1] is het beschikbare bewijs voornamelijk observationeel. In het grootste beschreven cohort (n=316) werd bij een gemiddelde koolhydraatinname van circa 36 gram per dag een gemiddelde HbA1c van 39 mmol/mol gerapporteerd. De frequentie van ernstige hypoglykemie bedroeg 2% en van diabetische ketoacidose 1% in het voorafgaande jaar [12]. De studie was gebaseerd op zelfrapportage zonder controlegroep, waardoor causale conclusies niet mogelijk zijn.
Naast cohortgegevens zijn meerdere peer-reviewde casusbeschrijvingen gepubliceerd van volwassenen met DM[1] die langdurig een ketogeen of zeer koolhydraatarm voedingspatroon toepasten. In een tienjarige n=1 follow-up werd een HbA1c van 37 mmol/mol gerapporteerd, met een Time in Range van 90% en een reductie van de totale dagelijkse insuline met circa 43%, zonder ernstige hypoglykemie of diabetische ketoacidose tijdens follow-up [34].
Een casus in Endocrinology, Diabetes & Metabolism Case Reports (2023) beschrijft eveneens substantiële reducties in insulinebehoefte bij toepassing van een ketogeen dieet, waarbij systematische keton- en glucosemonitoring centraal stond om metabole veiligheid te waarborgen [35].
In Clinical Diabetes (2025) werd een 32-jarige man beschreven die, na overstap op een ketogeen dieet in combinatie met hybride closed-loop insulinetherapie en tweemaal daagse capillaire ketonmeting, binnen drie maanden een HbA1c van 40 mmol/mol (5,8%) bereikte, met een gemiddelde glucose van 5,9 mmol/L en 99% Time in Range over een 14-daagse CGM-periode. Bij verdere follow-up werd zelfs 100% Time in Range gerapporteerd, met een HbA1c van 32 mmol/mol (5,1%) en een daling van de totale dagelijkse insulinebehoefte met ongeveer een derde. De auteurs benadrukken dat deze aanpak uitsluitend onder nauwe medische supervisie en met systematische ketonmonitoring dient te worden toegepast [36].
Andere individuele casussen beschrijven eveneens substantiële glykemische verbeteringen. Zo werd bij een 39-jarige vrouw een daling van HbA1c van circa 83 mmol/mol naar 58 mmol/mol gerapporteerd, met duidelijke afname van glykemische variabiliteit en psychosociale belasting in samenhang met ketogene voeding en pomptherapie [37].
In een afzonderlijk rapport werd bij een 19-jarige man op een paleolithisch ketogeen voedingspatroon een HbA1c van ongeveer 36 mmol/mol gemeten, met behoud van endogene C-peptideniveaus gedurende meerdere maanden, een uitzonderlijke individuele bevinding die niet generaliseerbaar is [38].
Deze casusbeschrijvingen tonen dat zeer lage koolhydraatinname bij geselecteerde volwassenen met DM[1] kan samengaan met uitzonderlijk stabiele glucosewaarden en substantiële reducties in insulinegebruik. Tegelijkertijd betreft het individuele of intensief gemonitorde situaties. Grootschalige, langdurige gerandomiseerde studies ontbreken, waardoor de reproduceerbaarheid en veiligheid op populatieniveau nog niet definitief zijn vastgesteld.
7. Risico’s en aandachtspunten van therapeutische koolhydraatbeperking bij diabetes type 1
Voor mensen met DM[1] vraagt TKB een zorgvuldige klinische benadering. Bij sterke koolhydraatreductie zijn met name ketoninterpretatie, voedingskwaliteit en lipidenrespons relevante aandachtspunten.
Ketoninterpretatie en risico op DKABij sterke koolhydraatreductie kunnen ketonen stijgen als fysiologische reactie op een lagere koolhydraatinname. Dit wordt vaak gezien bij vasten, inspanning of een ketogeen voedingspatroon en betekent op zichzelf geen ontregeling.
Diabetische ketoacidose (DKA) daarentegen ontstaat door een ernstig tekort aan insuline. Daarbij zijn ketonen verhoogd in combinatie met duidelijke hyperglykemie en metabole acidose. Klinisch gaat dit gepaard met klachten zoals misselijkheid, braken, buikpijn, diepe ademhaling en sufheid.
De interpretatie van ketonen vraagt daarom altijd om context. Een ketonwaarde van bijvoorbeeld 1,0 – 2,0 mmol/L bij normale glucosewaarden (4 – 8 mmol/L) en afwezigheid van klachten past bij fysiologische ketose (euketonemie; circa 0.5 – 3.0 mmol/L). Ketonen >3,0 mmol/L in combinatie met glucose >15 mmol/L en klinische symptomen wijzen op een mogelijk beginnende DKA en vereisen onmiddellijke actie.
Ketonmeting moet bij koolhydraatreductie daarom altijd worden geïnterpreteerd in samenhang met glucosewaarden, klachten en insulinegebruik. Alleen de ketonwaarde op zichzelf is onvoldoende om een klinisch oordeel te vellen [39].
Infobox: fysiologische ketose ≠ diabetische ketoacidose (DKA)
Kenmerk | Fysiologische ketose | Diabetische ketoacidose (DKA) |
Oorzaak | Vasten, inspanning, ketogeen dieet | Ernstig insulinetekort |
Glucosewaarden | Normaal (4-8 mmol/L) | Verhoogd (>15 mmol/L) |
Ketonen | Normaal of licht tot matig verhoogd (0,5–3,0 mmol/L) | Hoog (>3,0 mmol/L) |
pH-waarde bloed | Normaal (≥7.35) | Verlaagd (<7.30) |
Symptomen | Geen klachten, soms meer energie of alertheid | Misselijkheid, braken, buikpijn, diepe ademhaling, zoet ruikende adem, dorst, verwardheid, coma mogelijk |
Actie nodig? | Nee, tenzij klachten of ziekte | Ja, onmiddellijke medische interventie vereist |
Voedingskwaliteit en micronutriëntenTKB betekent per definitie een verschuiving in voedselkeuzes. Onderzoek laat zien dat lagere koolhydraatinname in onzorgvuldig samengestelde patronen gepaard kan gaan met lagere inname van micronutriënten zoals magnesium, calcium, folaat en vitamine C [40].
Analyses van zorgvuldig samengestelde laag-koolhydraatmenu’s tonen echter aan dat micronutriënten van vrijwel alle typen haalbaar zijn als de basis bestaat uit onbewerkte producten met een goede voedingsmatrix (groenten, eiwitten, gezonde vetten) [41–43]. Richtlijnen benadrukken daarom het belang van een volwaardig voedingspatroon en de kwaliteit van de producten. Professionele begeleiding, bijvoorbeeld door een diëtist met expertise in DM[1] wordt aanbevolen [6].
Lipidenrespons (met name LDL-cholesterol)Een klein deel van de mensen die een zeer koolhydraatarm voedingspatroon volgt, krijgt te maken met een stijging van LDL-cholesterol samen met gunstige veranderingen in andere metabole markers (zoals triglyceriden en HDL-cholesterol). Onderzoekers bespreken profielen zoals in de zogenoemde lean mass hyper-responders waarbij LDL-stijging meer uitgesproken kan zijn. Dit fenomeen is onderwerp van onderzoek; de klinische betekenis is nog niet duidelijk en moet individueel worden beoordeeld [44,45]. Gezien het cardiovasculaire risico bij DM[1] blijft monitoring van het lipidenprofiel onderdeel van integrale zorg, vooral bij sterke reductie van koolhydraten.
8. Klinische randvoorwaarden voor implementatie
TKB bij DM[1] is geen algemeen leefstijladvies, maar een interventie met directe gevolgen voor insulinebehoefte, glykemische dynamiek en metabole parameters Implementatie vraagt daarom een gestructureerde, gepersonaliseerde aanpak binnen reguliere diabeteszorg [6,46].
Aanpassing van insulinetherapieBij substantiële koolhydraatreductie verandert het glucose verloop na de maaltijd. Zowel de basale als maaltijdinsuline kunnen herziening vereisen. Lagere koolhydraatinname gaat vaak gepaard met een daling van de totale dagelijkse insulinebehoefte, terwijl maaltijden relatief rijk aan vet en eiwit een vertraagde glucose-respons kunnen geven [46,47]. Onvoldoende aanpassing vergroot het risico op hypo- en hyperglykemie.
Continue glucosemonitoring (CGM)CGM ondersteunt veilige implementatie door inzicht te geven in Time in Range, glykemische variabiliteit en vertraagde glucosestijgingen na de maaltijd. Dit is zeer relevant bij verandering van macronutriëntverdeling [46].
LipidenmonitoringBij sterke koolhydraatreductie kan bij een deel van de patiënten een stijging van LDL-cholesterol optreden [44,45]. Gezien het verhoogde cardiovasculaire risico bij DM[1] is periodieke controle van het lipidenprofiel aangewezen [46].
KetonenbeleidBij ziekte, stijgende glucosewaarden of malaise dient laagdrempelig ketonen te worden gemeten conform bestaande richtlijnen [39,46]. Het onderscheid tussen fysiologische ketose en diabetische ketoacidose is beschreven in paragraaf 7; interpretatie vereist altijd klinische context.
8.1 Extra voorzichtigheid
HbA1c >85 mmol/molBij mensen met een HbA1c boven de 85 mmol/mol vraagt het tempo van glykemische regulatie extra aandacht. Een snelle daling kan in zeldzame gevallen leiden tot verslechtering van retinopathie, een fenomeen dat ook is beschreven bij andere vormen van intensieve glucosecontrole [10]. Geleidelijke optimalisatie verdient daarom de voorkeur.
Gebruik van SGLT2-remmersSGLT2-remmers verhogen het risico op normoglykemische ketoacidose [8] en zijn daarom relatief gecontra-indiceerd bij diabetes type 1. In specifieke situaties, bijvoorbeeld bij hartfalen of nierschade, kan gebruik worden overwogen. Wanneer SGLT2-remmers worden gecombineerd met sterke koolhydraatreductie is een expliciete risicoafweging noodzakelijk, met een individueel veiligheidsplan inclusief ketonenbeleid en duidelijke afspraken over tijdelijke onderbreking bij ziekte of verminderde inname [48].
Kinderen en adolescentenEr heerst internationale consensus dat kinderen met DM[1] geen sterke koolhydraatbeperking zouden moeten volgen vanwege risico’s op groeiachterstand, hypoglykemie, verminderde werking van glucagon bij hypoherstel, cardiovasculaire gevolgen en eetstoornissen [49, 50]. Indien gezinnen toch kiezen voor een koolhydraatarm voedingspatroon, vereist dit intensieve begeleiding en monitoring van groei, voedingskwaliteit en psychosociaal functioneren [51].
9. Conclusie
TKB bij DM[1] is geen nieuwe ontwikkeling, maar een benadering met historische wortels die in het huidige tijdperk van continue glucosemonitoring en gepersonaliseerde zorg opnieuw klinisch wordt geëvalueerd. De beschikbare literatuur beschrijft dat zowel matige als sterke koolhydraatreductie gepaard kan gaan met meer Time in Range, minder glykemische variabiliteit en een lagere dagelijkse insulinebehoefte. In individuele en intensief gemonitorde situaties worden zeer stabiele glucosewaarden gerapporteerd en waarden richting normoglykemie benoemd.
Hoewel het bewijs grotendeels bestaat uit kleine interventiestudies, observationele cohorten en casusrapporten, zijn de beschreven effecten klinisch relevant. De hernieuwde belangstelling onder mensen met DM[1] weerspiegelt een behoefte aan strategieën die glucosefluctuaties beperken en de dagelijkse zelfmanagementbelasting verminderen.
TKB kan binnen de kaders van persoonsgerichte zorg worden overwogen als onderdeel van een gepersonaliseerd behandelplan, mits insulinetherapie zorgvuldig wordt aangepast en monitoring structureel is ingebed.
10. Meer lezen
Ervaringsverhalen
Voor lezers die zich meer willen verdiepen in de toepassing van koolhydraatreductie bij DM[1] in dagelijkse context, zijn verschillende ervaringsgerichte artikelen beschikbaar:
11. Meer bekijken
Webinar met Ian Lake, MD over therapeutische koolhydraatbeperking bij diabetes type 1
In dit webinar gaan huisarts Ian Lake en Amber Heijneman in gesprek over de rol van therapeutische koolhydraatbeperking bij diabetes type 1. Beide leven zelf met diabetes type 1.
Ian deelt zijn persoonlijke ervaringen met een ketogeen voedingspatroon en bespreekt hoe deze aanpak kan bijdragen aan stabielere bloedsuikerwaarden, minder hypo’s en een betere afstemming van insuline. Ook komen praktische vragen uit het dagelijks leven met diabetes type 1 aan bod, zoals de honeymoonfase, insulineresistentie en de uitdagingen van leefstijlverandering.
Recent werd een internationale evidence-based praktijkgids gepubliceerd voor diëtisten en voedingsprofessionals die therapeutische koolhydraatbeperking bij diabetes type 1 willen begeleiden. Deze gids, ontwikkeld door een internationaal team van clinici en onderzoekers, biedt praktische handvatten voor voedingssamenstelling, insuline-aanpassing en monitoring. Hoewel het geen formele richtlijn betreft van ADA of EASD, weerspiegelt het document de groeiende behoefte aan gestructureerde implementatie binnen een professioneel kader. Download de gids
12. Veelgestelde vragen (FAQ)
Auteur


Nieuwsbrief
Ontvang tips, nieuwe artikelen en inspiratie voor een gezondere leefstijl.
Gerelateerde artikelen
 Artikel
Artikel‘Het ketogeen eten maakt mijn diabetes controleerbaar’
Een ketogeen dieet en diabetes type 1, hoe gaat dit samen? Arjan Gunst deelt hoe het dieet hem helpt zijn bloedsuiker te stabiliseren en complicaties voorkomen.
 Artikel
Artikel‘Ik vertrouwde mijn lichaam niet meer en dat had impact op mijn mentale gezondheid’
Na haar LADA-diagnose kon Leonie van Someren niet meer van het leven genieten. Lees hoe ze met de dokter Bernstein-methode haar leven terugkreeg.
 Artikel
Artikel‘De koolhydraten die ik niet neem hoef ik ook niet te corrigeren met insuline’
Mart Snoek heeft diabetes type 1. Lees hoe hij balans vindt in een koolhydraatarm dieet, vasten, veel sporten en een do-it-yourself loop-systeem.
